Wenn Tier -, Insekten-oder menschliche Embryonen wachsen in einem unterernährten Umwelt, Ihrer der Entwicklung des Nervensystems bekommen Sie erste Wahl für alle verfügbaren Nährstoffen, so dass neue Neuronen gemacht werden können.
In diesem Prozess, das sogenannte organ-sparing -, Ressourcen werden bevorzugt Delegierten des Nervensystems auf Kosten der weniger wichtigen Organen oder Geweben.
Neue Forschung zeigt nun, dass in der Entwicklung des Nervensystems zeigen das bevorzugte Wachstum auch auf der Ebene der einzelnen Neuronen. In einer Veröffentlichung in eLife Juni 22, „Low FoxO-expression in Drosophila somatosensorischen Neuronen schützt Dendriten-Wachstum unter Nährstoff Einschränkung,“ ein team von der Cornell-Forscher entdeckt den molekularen Mechanismus, der hilft, erleichtern organ-sparing auf diese Zelle-für-Zelle-basis.
„Die Phänomene, die wir gefunden haben, ist ähnlich wie die Phänomene der Schonung des Gehirns, aber es gibt sehr wichtige Unterschiede“, sagte Chun Han, senior-Autor und Nancy M. und Samuel C. Fleming Associate Professor in der Abteilung der Molekularbiologie und Genetik in der Hochschule für Landwirtschaft und Life Sciences und in der Weill-Institut für Zell-und Molekularbiologie. „Die Nervenzellen werden geschützt, das Wachstum der Ebene der einzelnen Neuronen, und Sie werden größer und größer durch Strecken Ihre äste.“
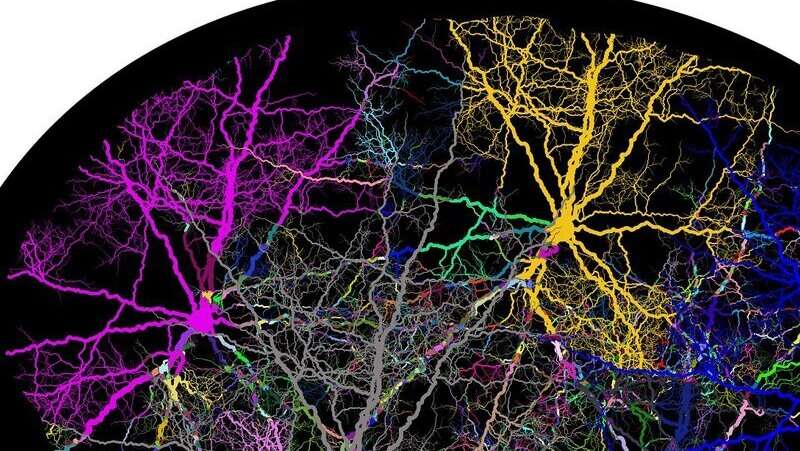
Diese Zweige sind Dendriten. Sie bilden ein system von aufwendigen Arme, die sich von Neuronen “ zelluläre Körper, und Sie kann empfangen Reize aus der äußeren Umwelt.
Han und sein team wollten prüfen, wie Nährstoff-Mangel wirkt sich auf die Dendriten Wachstum von einzelnen Neuronen, und dann untersuchen, welche zellulären Opfer Körper machen, so dass lebenswichtige Organe, einschließlich das Gehirn, weiter zu entwickeln.
Sie teilten Drosophila (Frucht-Fliegen) Larve in Gruppen, welche entweder ein high – oder low-Hefe-Diät, die Simulation von nährstoffreichen und nährstoffarmen Umgebungen. Dann beobachteten Sie, wie neuronale Zellen entwickelten sich im Vergleich zu den benachbarten Hautzellen auf dem Körper Wand. Sie überwacht die Fortschritte, die alle 24 Stunden mit der konfokalen Mikroskopie, die Laser verwendet, um Licht fluoreszierende Marker, die Beschriftung der einzelnen Zellen.
„Wir haben sehr schöne Marker, die spezifisch die Kennzeichnung dieser Populationen von Neuronen,“ Han sagte. „Jedes neuron ist uns klar—bis hin zu jedem einzelnen Zweig.“
Die Forscher beobachteten, dass die Neuronen wuchs bei einer viel höheren rate als die Haut, die Zellen in der niedrig-Hefe-Umgebung. Hautzellen schneller gewachsen, als es noch weniger Konkurrenz um Nährstoffe. Han und seinem team gelernt, dass dieser Unterschied durch eine kritische gen namens FoxO—ein wichtiger regulator der zellulären stress-Antwort.
„FoxO ist ein gen, das drückt sich in so ziemlich den meisten Zellen des Körpers,“ Han sagte. „Wenn die Zellen Gesicht, low-Nährstoffe, FoxO stellt eine Bremse für das system und verlangsamt das Wachstum von Zellen.“
Was ist besonders interessant an FoxO, dass gerade da die meisten Zellen haben, bedeutet nicht, Sie alle nutzen es zur gleichen Zeit oder unter den gleichen Bedingungen. Han s-team entdeckt, dass auch während der fehl-und Mangelernährung, die Drosophila Neuronen exprimiert sehr wenig FoxO, in der Erwägung, dass die epidermalen Zellen exprimierten FoxO-auf weit höherem Niveau.
Wenn es weniger Nährstoffe zur Verfügung, FoxO löst eine Reaktion in den epidermalen Zellen, die sogenannten autophagie, was sagt die Zelle selbst zu zerstören durch den Verzehr selbst. Jedoch beschränkt sich der FoxO-expression in Neuronen bewahrt einzelnen neuronalen Zellen und Ihre Dendriten Wachstum.
Und während die Menschen haben komplexere Systeme als Drosophila, Han sagte, dass diese Forschung hilft den Weg ebnen für die Untersuchung ähnliches Phänomen beim Menschen.
