Die schnelle Kommunikation von Nervenzellen im Gehirn, sowie die Fähigkeit, zu lernen, fundamental angewiesen auf die neurotransmitter-Rezeptoren befindet sich in den Kontaktstellen der Nervenzellen, den Synapsen. Die wichtigsten Rezeptoren im Gehirn von Säugetieren sind die Glutamat-Rezeptoren des AMPA-Typs (AMPAR), die Erzeugung des elektrischen Signals erforderlich für eine schnelle Kommunikation zwischen den Neuronen. Die Anzahl der AMPARs moduliert wird, durch den Grad der synapse Aktivität: Wie lernt es, die Anzahl der AMPARs erhöht, wodurch die synaptische Signalübertragung zuverlässiger und fahren synaptische Plastizität fördert die Gedächtnisbildung. Grundlegende Voraussetzung für diese synaptische Plastizität ist die effiziente Montage von AMPARs aus verschiedenen protein-Untereinheiten im endoplasmatischen Retikulum (ER) der Nervenzellen, für die keine oder nur wenig Informationen zur Verfügung, so weit.
Für die erste Zeit, ein team von Neurobiologen aus Freiburg unter der Leitung von Prof. Dr. Bernd Fakler vom Institut für Physiologie in Zusammenarbeit mit Kollegen der Goethe-Universität Frankfurt und des Max-Planck-Institut für Medizinische Forschung in Heidelberg, konnte zeigen, dass AMPARs sind zusammengesetzt aus Haupt-und Hilfs-Untereinheiten in einer Schritt-für-Schritt-Prozess, ähnlich wie auf einem Fließband. Die einzelnen Etappen durchgeführt werden, von anderen ER-Residenten Proteinen und protein-komplexen. Störung der Versammlung durch Mutationen in der Montage-Elemente im Menschen oder durch Ihre gezielte genetische Inaktivierung—knock-out—Mäusen, führt zu einer massiven Beeinträchtigung der synaptischen Signaltransduktion und lernen. Umgekehrt, der Anstieg der rezeptor-Produktion durch überexpression von Fließband-Proteine führt zu einer erhöhten Plastizität der Synapsen. Die Wissenschaftler kürzlich veröffentlichte diese Ergebnisse in der Zeitschrift Neuron.
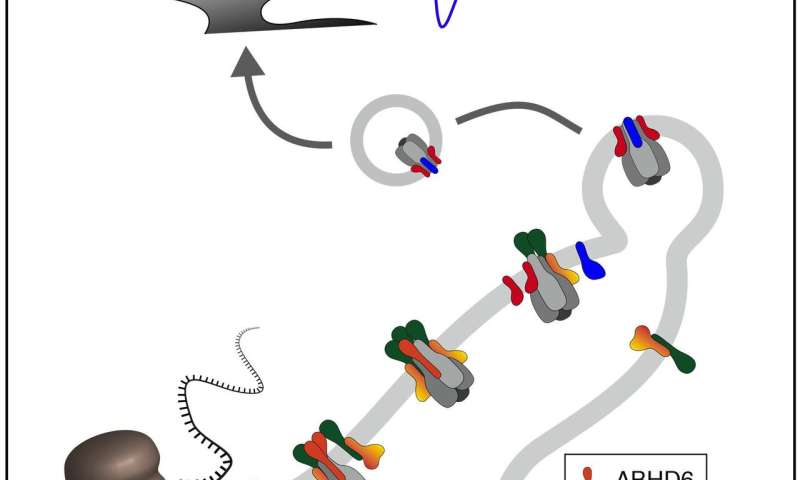
Mit hoch auflösenden Proteom-Techniken, haben die Forscher identifizierten Proteine im ER-Membranen der Neuronen, die erforderlich sind für die Montage von funktionalen AMPARs von vier pore-forming Untereinheiten und vier Hilfs-Untereinheiten: Der erste Baustein, die Proteine ABHD6 und PORCN, schützt den einzelnen pore-forming GluA Untereinheiten von vorzeitiger Abbau. Der zweite Baustein, ein Komplex von den Proteinen, FRRS1l und CPT1c, versammelt vier GluA-protein in einem rezeptor-Kanal und bereitet Ihren Verein mit den vier Hilfs-Untereinheiten, die cornichon-oder TARP-Proteine. Dieser Letzte Schritt distanziert sich die FRRS1l-CPT1c Komplex und ermöglicht den export der funktionalen AMPARs von dem ER und Ihr transport in die Synapsen.
Die einzelnen Schritte entlang dieser Montagelinie sind genau abgestimmt und optimiert für die effiziente Montage der Rezeptoren. Wenn der Betrieb der Montage-Linie gestört wird, beispielsweise durch mutation-damit verbundenen Verlust der Funktion der FRRS1l Eiweiß, dies führt zu schweren Funktionsstörung des Gehirns beim Menschen, wie beschrieben, das die Forscher in einer früheren Arbeit 2017: Alle Patienten zeigten eine stark eingeschränkte Intellektuelle Fähigkeiten, die mit IQ-Werten unter 40, verzögerte oder fehlende Sprachentwicklung und eine erhöhte Tendenz für epileptische Anfälle.
