Die Schaffung neuer Blutgefäße, ein Prozess, der als Angiogenese bei Tumoren in den Lymphknoten ist, anders als bei Tumoren in anderen teilen des Körpers, wie den Darm oder die Lunge, ein team vom Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC) berichten in der Fachzeitschrift Cancer Research. Wissenschaftler des MDC-Labore von Dr. Armin Rehm, Dr. Uta Höpken und Professor Holger Gerhardt waren in dieses Projekt involviert. Das team identifiziert, die möglicherweise wirksamere Behandlung Ziele zu verlangsamen tumor-Wachstum für Lymphom-Patienten.
Lymphom ist Krebs des lymphatischen Systems, die auch die Lymphknoten, die Milz und Knochenmark. Lymphom-Patienten mit Indikatoren erhöhter Blutgefäß-Entwicklung haben in der Regel geringere überlebenschancen. Sie auch don ‚ T reagieren gut auf die Behandlungen, die erfolgreich gehemmt Blutgefäß-Entwicklung in anderen Krebsarten.
„Wir stellten die Hypothese, dass Tumoren in den Lymphknoten sind völlig Verschieden von soliden Tumoren, weil die Lymphknoten so unterstützend mikroumgebung für durch Blut übertragbare tumor-Zellen“, sagt Dr. Uta Höpken, Leiter der MDC Umweltbedingten Regulierung in Autoimmunität und Krebs Lab. Trotzdem, es war „völlig überraschend, dass keiner der üblichen verdächtigen beteiligt waren“, sagte Dr. Armin Rehm, wer führt MDC Translationale Tumorimmunology Lab.
Beseitigung von verdächtigen
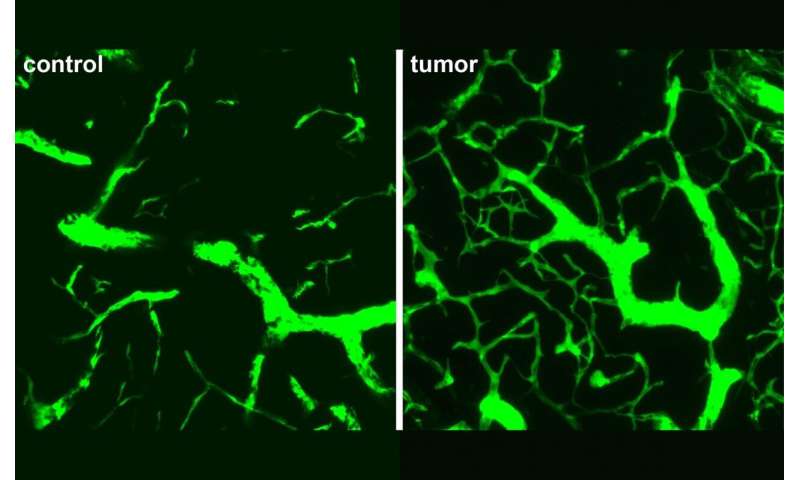
Blutgefäße in der frühen Lymphom sind ungewöhnlich dicht und unregelmäßig, mit viel mehr Verzweigungen als beobachtet in Blutgefäßen von gesunden Lymphknoten. Das Muster der Verzweigung wurde nicht beobachtet, in soliden Tumoren in infizierten Lymphknoten oder in die Entwicklung von Organen, die in der Regel anderen Seiten der neo-Angiogenese.
Zu entdecken Sie die einzigartige Signalwege, die Antrieb dieser Entwicklung, das team lief Analysen mit transgenen Mausmodellen, die die Entwicklung von Lymphomen, sowie Mäuse mit implantierten Lymphom-Krebs-Zellen. Sie blickte auf gen-Expressionsmuster zu sehen, welche Gene und Proteine sind am aktivsten in der Anfangsphase der tumor-Entwicklung.
Täter in der Regel impliziert in die tumor-Angiogenese—Entzündung, niedrige Sauerstoff-Niveaus, und die Signalisierung zwischen der Basis und an der Spitze der Blutgefäße, die sogenannten Notch-Signalweg—nicht zeigen, bis in den Ergebnissen.
Erfolgreiche blocks
Eine Gruppe von Proteinen, die sogenannten vascular endothelial growth factor (VEGF), sind als primäre Treiber der normalen Blutgefäß-Entwicklung als auch in der Angiogenese in Tumoren. In den meisten festen Masse Tumoren, VEGF-A das protein ist Vermittlung der Prozess, in Verbindung mit seinem rezeptor, genannt VEGFR-2.
In den frühen Stadien des Lymphoms, das team entdeckte VEGF-C ist die aktive protein. Wenn Sie versucht, zu blockieren rezeptor VEGFR-2 zu hemmen VEGF-C-Aktivität, nichts geändert.
Aber wenn die Forscher blockiert einen anderen rezeptor, VEGFR-3, Blut-Gefäß-Wachstum deutlich verlangsamt. Sie auch unterbrochen, ein rezeptor für ein kleines protein namens lymphotoxin, die in der Regel notwendig, für den normalen Lymphknoten Entwicklung auch geholfen, langsam Angiogenese.
Das team verwendet zwei Medikamente, die bereits genehmigt sind, für die klinische Anwendung bei Autoimmun-Erkrankungen zu hemmen, die Wege. Sie bestätigt die Behandlung, arbeitete auch auf die menschlichen Zellen. Während nicht die ärzte selbst, die Forscher hoffen, dass die Behandlung aufgenommen werden können, die für klinische Studien, um zu untersuchen, Ihre Wirksamkeit im menschlichen Patienten. „Wenn einige Krebszellen überleben, Chemotherapie, könnte es möglich sein, zu verhindern, dass Rückfall von der Bewältigung dieser Wege mit immunotherapy,“ sagte Rehm.
Gerade von der start
Ein wesentliches Merkmal dieser Studie war das timing. Die Forscher verfolgt die Angiogenese in den ersten zwölf Tagen nach Krebszellen eingedrungen, Lymphknoten. Dies gab Ihnen eine einzigartige Gelegenheit zur Beobachtung der frühen „übersprechen“ oder die Interaktion zwischen Tumorzellen und den Lymphknoten-mikroumgebung. Nur fünf bis zehn Prozent der Lymphknoten-Zellen waren bösartig, und bereits die Lymphknoten wurde umstrukturiert. „Die Veränderungen, die wir sahen auftreten, sehr früh mit einer sehr geringen tumor burden,“ Höpken sagte.
Bildgebung diese frühen Veränderungen in hoher Auflösung präsentiert, eine Herausforderung, die viel Sorgfalt. „Lymphom-Zellen sind weit verbreitet innerhalb der Zellen hoch kompartimentierten Lymphknoten“, sagte Lutz Menzel, co-Erstautor und post-doc in der Translationalen Tumorimmunology Lab. „Suche nach Lymphom-bedingte Umbau von dem stroma, wenn in anderen Bereichen der Lymphknoten blieb unberührt, ganz oft wurde eine Suche nach einer „Nadel im Heuhaufen“ unter die Lupe.“
Das team Unterstrich die Bedeutung der Tiere für diese Arbeit. Eine solche Studie ist nicht möglich, mit menschlichen Patienten, weil Sie noch nicht zeigen Symptome. „Die Tiere bieten den Vorteil, zu sehen, was Los ist zu Beginn der Krankheit, anstatt das Ende,“ sagte Rehm. „Organoids sind einfach noch nicht weit genug entwickelt, um imitieren die Interaktionen zwischen vielen verschiedenen Zelltypen, die in komplexen Lymphknoten Gewebe.“
